
En ny undersøgelse offentliggjort i Aging Cell i 2025 giver et detaljeret indblik i, hvad der sker, når cellerne mister deres forsyning af NAD⁺, et af kroppens mest essentielle molekyler for energi og reparation.
Forskerne fandt bl.a. ud af, at når cellerne mister NAD⁺, bliver de ikke bare langsommere - de aktiverer en forsvarsmekanisme, der efterligner en virusinfektion, selv om der faktisk ikke er nogen virus til stede.
Indholdsfortegnelse
- Sådan undersøgte forskerne NAD⁺-tab
- Hvad disse resultater betyder
- Understøtter NAD⁺ for cellulær balance
Sådan undersøgte forskerne NAD⁺-tab
For at undersøge denne proces dyrkede forskerne fibroblastceller, som er en almindelig type bindevævscelle, i 14 dage i et miljø uden nikotinamid.
Hvad er nikotinamid?
Nicotinamid, som også går under navnet NAM, er en form for B3-vitamin, som kroppen bruger til at producere NAD⁺ - et vitalt molekyle, der er involveret i energiproduktion og cellulær reparation.
Gennem hele eksperimentet målte de:
- Mitokondriernes energiproduktion
- Oxidativt stress og antioxidant-aktivitet
- Genekspression relateret til immunitet
- Ændringer i mitokondrie-DNA's (mtDNA) placering i cellen.
Relateret: Hvad er NAD+? Et livsvigtigt molekyle for sundhed og longevity.
Formålet med undersøgelsen
Målet var at forstå, hvordan celler tilpasser sig - eller ikke tilpasser sig - under kronisk NAD⁺-udtømning. Forskerne ville se, hvordan tabet af dette vitale molekyle påvirkede energiproduktionen, stressresponsen og kommunikationen mellem mitokondrier og resten af cellen.
Lad os se nærmere på, hvad de opdagede, da cellerne begyndte at mangle NAD⁺.
Cellerne overlevede - men på minimal energi
Efter bare to dage uden nikotinamid faldt cellernes NAD⁺-niveauer til mindre end 5 % af det normale. Alligevel døde cellerne ikke - det lykkedes dem at overleve og fortsætte med at dele sig, men meget langsommere. Det viser, at fibroblastceller kan holde sig i live med meget lave NAD⁺, men de mister deres evne til at tilpasse sig og producere energi effektivt.
Mitokondrier mistede deres fleksibilitet
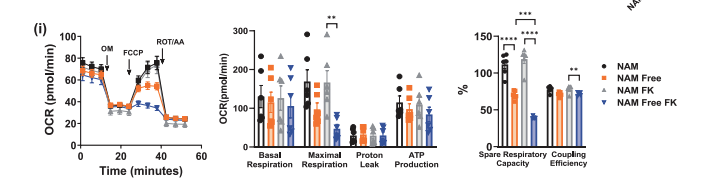
Mitokondrierne - de dele af cellen, der er ansvarlige for at producere energi - kunne stadig skabe en grundlæggende mængde energi, men de mistede evnen til at øge produktionen, når cellen havde brug for mere. Med andre ord var deres "energireserve" næsten væk. Både deres ekstra kapacitet og deres maksimale ydeevne faldt kraftigt. Da nikotinamid blev tilføjet igen, kom mitokondrierne hurtigt på fode igen, hvilket viser, at NAD⁺ er afgørende for at holde cellens energisystem kørende effektivt.
Stigende oxidativ stress
Celler med lavt NAD⁺ viste tydelige tegn på oxidativ stress - en tilstand, hvor skadelige molekyler ophobes hurtigere, end cellen kan fjerne dem. Det skaber en indre belastning og beskadiger langsomt vigtige cellekomponenter.
Forskerne fandt ud af, at tegnene på skader øgedes, mens cellernes naturlige forsvarssystem blev svagere. Normalt ville beskyttende enzymer blive mere aktive for at neutralisere stress, men i dette tilfælde forblev de inaktive.
Med andre ord
Cellerne producerede flere skadelige molekyler, end de kunne neutralisere. Deres interne "oprydningshold" reagerede ikke, hvilket gjorde dem mere udsatte for slitage - en proces, der er tæt forbundet med aldring og sygdom.
Mitokondrie-DNA slap ud i cytoplasmaet
En af de mest slående opdagelser var, at mitokondrierne begyndte at lække deres eget DNA ud i det omgivende cytoplasma.
Normalt forbliver mitokondrie-DNA sikkert låst inde i mitokondrierne. Men når NAD⁺-niveauerne faldt, lækkede små fragmenter ud i cellen. Cellen opfattede det som et tegn på infektion og aktiverede sit interne alarmsystem - kendt som cGAS-STING-stien.
Dette system reagerer normalt på virus ved at aktivere immungener, der producerer beskyttende molekyler kaldet interferoner. I dette tilfælde var der dog ingen virus til stede. Cellerne reagerede simpelthen på deres eget undslupne DNA og skabte en viruslignende inflammatorisk reaktion uden nogen egentlig infektion.
cGAS-STING-vejen
Et indbygget alarmsystem i cellerne, som opdager fejlplaceret DNA. Når det aktiveres, udløser det en immunrespons for at beskytte mod virus - men det kan også tænde under intern stress eller mitokondrie-skader.
VDAC1: Porten, der lukker DNA'et ud
Proteinet VDAC1 sidder i mitokondriernes yderste lag og fungerer som en lille port, der kontrollerer, hvad der kommer ind og ud. Når NAD⁺-niveauet faldt, åbnede porten sig og lod små stykker mitokondrie-DNA slippe ud i resten af cellen.
Da forskerne blokerede porten med et stof kaldet VBIT-4, stoppede både DNA-lækagen og immunreaktionen.
Det viser, at VDAC1 er det vigtigste bindeled mellem lav NAD⁺, ustabile mitokondrier og inflammation.
Reaktionen kan vendes om
Da forskerne genoprettede NAD⁺ ved at tilsætte nikotinamid (NAM), NMN eller nikotinamid-ribosid (NR), genvandt cellerne balancen. Mitokondrierne blev stabiliseret, det oxidative stress faldt, og den antivirale immunaktivering forsvandt. Effekten var fuldt reversibel og direkte afhængig af tilgængeligheden af NAD⁺.
Oversigt
| Observation | Effekt |
|---|---|
| Lave NAD⁺-niveauer | Udløste et viruslignende immunrespons selv uden infektion |
| Mitokondrie-protein VDAC1 | Tillod mitokondrie-DNA at lække ind i cellen |
| Blokering af VDAC1 eller genoprettelse af NAD⁺ | Stoppede inflammation og stabiliserede cellefunktionen |
| Gendannelse af NAD⁺ (via NAM, NMN eller NR) | Omvendt alle negative effekter og genoprettet balance |
Hvad disse resultater betyder
Undersøgelsen viser, at når NAD⁺-niveauet falder, sænker cellerne ikke bare deres aktivitet - de udløser en falsk alarm. Mitokondrierne begynder at lække små stykker DNA gennem et gate-protein kaldet VDAC1, som får cellen til at tro, at den er under virusangreb. Det aktiverer en unødvendig immunrespons. Da forskerne enten genoprettede NAD⁺ eller blokerede porten, stoppede denne reaktion, og cellerne blev normale igen.
Selv om forskningen blev udført i cellekulturer, giver den en mulig forklaring på, hvorfor NAD⁺-niveauerne falder med alderen, og hvordan det kan bidrage til den langsomme, kroniske inflammation, der ofte ses i aldrende væv. Resultaterne afslører, hvor tæt vores energimetabolisme, mitokondriestabilitet og immunbalance hænger sammen.
Understøtter NAD⁺ for cellulær balance
Da NAD⁺-niveauerne blev genoprettet, aftog alle de skadelige reaktioner - hvilket viser, hvor vigtig en sund NAD⁺-metabolisme er for cellestabiliteten. NAD⁺-niveauer kan understøttes gennem ernæring, fysisk aktivitet og forstadier som NMN eller NR, som kroppen omdanner tilbage til NAD⁺.
Set i lyset af denne undersøgelse handler opretholdelse af NAD⁺ gennem smarte tilskud ikke kun om at øge energien - det handler om at hjælpe cellerne med at forblive modstandsdygtige, afbalancerede og beskyttede, når vi bliver ældre.
Relateret: 7 NAD+-forløbere: Hvad de er, hvordan de virker, og hvilke der ser mest effektive ud.
Ansvarsfraskrivelse
Denne blog er udelukkende baseret på de videnskabelige resultater, der er offentliggjort i Aging Cell (2025). Purovitalis fremsætter ingen produkt- eller sundhedsanprisninger i forbindelse med denne undersøgelse. Målet er at formidle forskningen på en evidensbaseret og letforståelig måde, så læserne kan lære af selve de videnskabelige data.
Referencer
- Chini CC, Camacho-Pereira E, Liu L, et al. Kronisk cellulær NAD-udtømning aktiverer en virusinfektionslignende interferonrespons gennem mitokondriel DNA-lækage. Aging Cell. 2025;24(9):e135

NMN-tilskud Europæisk baseret Liposomal levering
Vores NMN-tilskud er her for at hjælpe dig med at stråle og føle dig bedst mulig! Prøv det nu!

Boost dine NAD-niveauer nu
Oplev vores førsteklasses NAD+ booster , og styrk din vitalitet.













