Aging is something we all go through, and scientists have always been curious about it. As time goes on, our bodies don’t work as well as they used to. This means we might get sick more often or take longer to heal. Some of us might even face bigger health problems like heart diseases or cancer. A famous study called “The Hallmarks of Aging” listed nine main reasons why we age. Then, in 2022, researchers in Copenhagen added five more reasons to that list. All this research helps us better understand the changes happening in our bodies as we grow older.
At Purovitalis, we’re deeply invested in understanding these hallmarks of aging. We believe that by focusing on them, we can create supplements that truly support our bodies as we age. But we also know that science can be complicated. That’s why we’re committed to explaining these hallmarks in a way that’s easy for everyone to understand. Our goal is to bridge the gap between complex scientific concepts and everyday knowledge, ensuring you’re well-informed and confident in the choices you make for your health.

Let’s take a closer look at these 14 hallmarks to better understand what happens in our body during the aging process:

Think of your DNA as your body’s instruction manual. Genome instability can blur these instructions due to errors from DNA replication or cellular stress. While minor DNA damages aren’t always harmful, they can accumulate over time, causing cells to malfunction and contribute to aging.
If a cell has too many errors, especially in the mitochondria (the cell’s energy producers), it might not work efficiently. However, substances like Resveratrol, magnesium, vitamin B, melatonin, creatine, and NMN can support healthy mitochondrial function.
Think of your DNA as a shoelace, with telomeres resembling the small plastic tips at the ends. These telomeres protect our essential DNA.
Why are Telomeres Associated with Aging?
Telomeres prevent our DNA from sticking to other cellular components. If DNA is the body’s instruction manual, telomeres ensure these instructions remain separate and undamaged. They also regulate how often a cell can divide. As cells divide, telomeres shorten, acting like a countdown. When they become too brief, the cell stops dividing, which can lead to cell aging or damage. Some researchers believe this process might be tied to human aging. Preserving our telomeres could potentially extend our healthspan.
Epigenetic changes are like switches that can turn certain parts of our DNA on or off. They don’t change the DNA itself but can affect how it works. These changes can be influenced by our diet, stress, and things in our environment.
As we age, these switches can affect things like inflammation and how our cells produce energy. If too many switches are in the wrong position, it can make us age faster.
By understanding and managing these switches, we might be able to age more healthily. Simple things like eating well, reducing stress, and avoiding harmful habits like smoking can help keep these switches in the right position.
As we age, our bodies might struggle to keep proteins in check, leading to issues like inflammation and organ problems. If too many damaged proteins accumulate, it can speed up aging and cause diseases.
The good news? We can help our bodies manage proteins. Eating less, fasting, and following diets like the Mediterranean or DASH can help. Plus, living a stress-free life is essential, as stress can disrupt our protein balance and overall health.
A recent 2022 study from Copenhagen highlighted a new aspect of aging. The tiny organisms in our gut, known as the gut microbiome, undergo changes over time. There’s a shift in the type of microbes and a decrease in species variety. Additionally, barriers in our body, like the gut wall, can weaken, leading to inflammation. These alterations in gut health can result in inflammation that affects our overall well-being.
Maintaining a healthy gut can involve lifestyle changes such as eating healthy fats, drinking plenty of water, and staying active.


*These statements are not yet been officially established by the (European) authorities and are based on research articles.

Nutrient sensing is when our bodies manage the use and storage of the food we eat. In our youth, this system works efficiently, helping with energy and cell repair. But as we age, it can become less accurate. This can lead to issues like inefficient processing of sugars or fats, weight gain, and inflammation. When this system is off, it can also disrupt autophagy, our cells’ cleaning process. This disruption can speed up aging and lead to age-related diseases
Mitochondrial dysfunction relates to a decline in our cells’ energy production. When cells have ample nutrients, they store energy. When nutrients are scarce, cells focus on repair. However, sometimes cells don’t react properly due to issues with nutrient-sensing pathways. Some proteins play a role in cell metabolism and aging. One way to address this is by reducing calorie intake by 10% to 30%, ensuring essential nutrients are still consumed. This approach has been shown to boost health and longevity.
Mitochondria, our cells’ powerhouses, produce most of the energy we need. But this process also releases harmful particles called free radicals. Over time, these particles damage the mitochondria, leading to less efficient energy production, DNA damage, and protein imbalances. As we age, we also have fewer mitochondria, contributing to muscle weakness and a less robust immune system.
Senescent cells are old or damaged cells that stop dividing and no longer help the tissues where they live. These cells not only become inactive but also send harmful signals that can turn healthy cells senescent too. Over time, as more of these senescent cells build up, they can cause problems in our body. They can make our tissues stiff, reduce their function, and lead to age-related diseases.
In simple terms, while having some old cells is natural, too many of them can speed up the aging process and cause health issues.
Inflammation is a key sign of aging, often referred to as “inflammaging.” As we grow older, a constant, low-level inflammation can develop, which is linked to many age-related diseases. Researchers believe this type of inflammation is so significant that it deserves special attention when discussing aging factors. This inflammation doesn’t just stand alone; it can affect other aspects of our health, including cell behavior and gut balance. While there are substances like green tea extracts and ginger that might help manage inflammation, it’s essential to understand its role in the aging process.

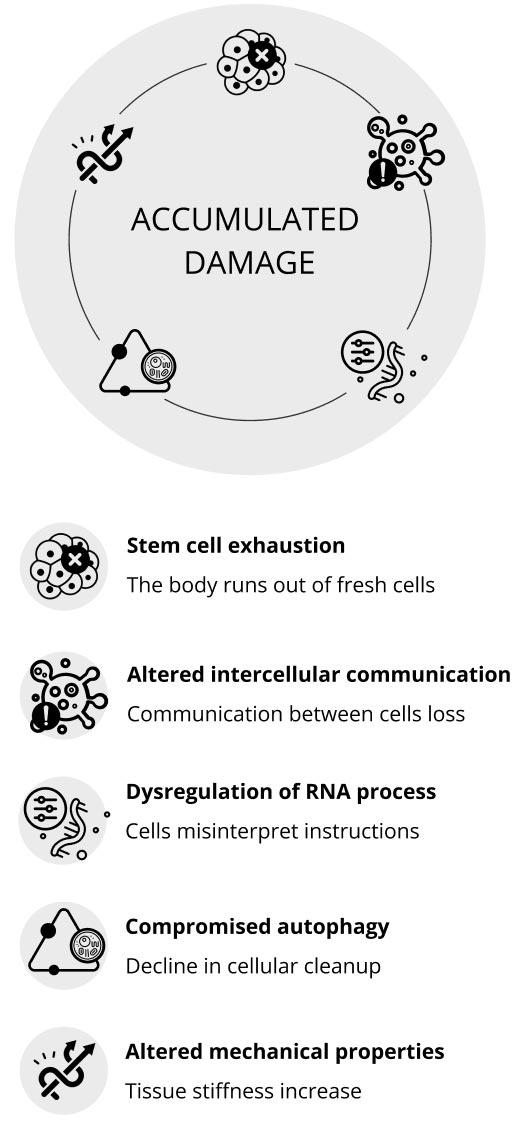
Stem cells, fresh and blank, wait for signals to decide their type and function, making them especially useful in replacing damaged cells in our body. These undifferentiated cells can transform into necessary cell types and assist in maintaining our body’s health.
However, senescent cells, old and non-working, emit signals that cause inflammation and can reduce stem cell activity, impacting our immune system and our tissue’s ability to regenerate. Also, issues like the shortening of their telomeres and genetic changes can negatively affect their functionality over time.
Our cells’ ability to communicate with each other can decline over time, leading to what’s known as altered intercellular communication. Picture it like phones with bad reception, causing misunderstandings between cells. This “static” makes cells send out “SOS” signals when they shouldn’t. These mixed signals can result in inflammation and a weakened immune system, increasing our vulnerability to health issues.
Splicing dysregulation is a hallmark of aging that refers to the disruption in how cells process RNA, a molecule vital for translating our genetic code into functional proteins. RNA splicing is like editing a film, where unnecessary clips are removed to create a coherent story. As we age, this “editing” process can become less precise, leading to the production of incorrect or non-functional proteins. These protein anomalies can disrupt cellular functions, contribute to abnormal cell behaviors, and accelerate the aging process. Understanding splicing dysregulation is crucial because it offers insights into age-related diseases and the broader mechanisms of aging.
Compromised autophagy is a hallmark of aging. Think of autophagy as our body’s housekeeping service, responsible for tidying up and recycling damaged cell components. However, as time goes on, this cleanup process becomes less effective. This decline in cellular housekeeping is linked to age-related concerns, including cognitive decline and a less responsive immune system.
Studies have shown that boosting autophagy can extend the lifespan in mice and enhance the effectiveness of vaccines in older populations by rejuvenating their immune response.
Aging relates to shifts in cells and their surrounding environment. For instance, fibroblast cells change their inner structure as they age, which affects their movement and communication with other cells. These changes, especially in the aging immune system, can damage tissue and harm health. Moreover, the nucleus of a cell, an essential part, changes during aging and can kickstart more cell aging processes. Treatments stabilizing this cell part can extend lifespan in certain conditions that speed up aging. Also, the environment outside of the cell loses flexibility and gets stiffer as we age, leading to various age-related problems and diseases.


We age due to the cumulative effects of the 12 hallmarks, like DNA damage (genomic instability), telomere shortening, and mitochondrial dysfunction. These processes impair cell repair and function over time, driven by genetic, environmental, and lifestyle factors, leading to physical decline and disease.
No, aging varies across species. While mammals experience hallmarks like telomere attrition and senescence, some organisms (e.g., certain jellyfish or hydra) show negligible senescence, maintaining cell renewal indefinitely. Even among mammals, rates differ—mice age faster than humans due to variations in repair mechanisms and metabolism.
Yes, studying species with unique aging traits, like negligible senescence in lobsters or hydra, can reveal mechanisms to slow human aging. For example, research on naked mole rats, which resist cancer and live longer than expected, highlights enhanced DNA repair and proteostasis. These insights could inform interventions targeting hallmarks like genomic instability or cellular senescence, potentially leading to therapies that extend human healthspan.
The hallmarks of aging are 12 biological processes, like genomic instability, telomere attrition, and mitochondrial dysfunction, that drive age-related decline and disease. They interact to accelerate aging.
These hallmarks cause cellular and tissue damage, leading to diseases like cancer, Alzheimer’s, and heart disease, while reducing overall vitality and lifespan.
While not fully reversible, interventions like exercise, caloric restriction, and supplements (e.g., NMN) can slow or mitigate some hallmarks, such as cellular senescence or mitochondrial dysfunction.
Chronic inflammation, or “inflammaging,” damages tissues and promotes diseases like arthritis and diabetes by disrupting cellular communication and amplifying other hallmarks.
A balanced diet, rich in antioxidants and nutrients, supports proteostasis, reduces inflammation, and boosts autophagy, helping to counteract aging processes.
NMN boosts NAD+ levels, supporting nutrient-sensing pathways and mitochondrial function, which may slow hallmarks like deregulated nutrient sensing and energy decline.
Regular exercise, stress management, quality sleep, and intermittent fasting can enhance autophagy, reduce senescence, and improve stem cell function to promote healthy aging.
We’re here to make healthy living effortless. Cookies help our website perform at its best and allow us to understand how we can improve your experience with Purovitalis. Privacy Policy • Imprint
These cookies keep the website running — things like your shopping cart, checkout, and security settings. Without them, the site wouldn’t work properly.
These help us remember your choices and improve your experience, like showing the right language or survey questions that fit your interests.
These cookies show us how visitors use our site so we can make it faster, clearer, and more useful. All data is collected anonymously.
These help us share relevant offers and information about Purovitalis across other websites and platforms — so you see content that matters to you.








Start Plans include 3 monthly deliveries and continue monthly after that unless canceled.
Before 3 deliveries
You can cancel at any time, but the plan will remain active until all 3 monthly deliveries are completed.
After 3 deliveries
You can cancel at any time before your next renewal. The plan does not end automatically and must be canceled manually.
Pausing or rescheduling
You can pause or change your delivery date at any time from your account.
Returns & refunds
Subscription orders are not eligible for refunds once shipped. Products already delivered as part of a Start Plan cannot be returned.
You can manage your plan anytime via My Account → Subscriptions, or contact us at [email protected].
Sign up for a 7-day free trial of our AI-powered app and take the first step towards a younger, healthier you.
or get full access with your product subscription!
Prof. Dr. Andrea Maier is an internist and professor of aging (“ longevity medicine ”) at the Vrije Universiteit in Amsterdam and the University of Melbourne, Australia. She studies the aging body and searches for anti-aging treatments. She heads the Center for Healthy Longevity in Singapore.
Why do we gradually decline during our average life of more than 80 years? Can we stop that process? Or maybe even turn around? And to what extent should we really want that? Maier gives practical tips on how we can extend our lifespan while also staying healthy.
Andrea Maier graduated in Medicine from the University of Lübeck in 2003. She specialized in internal medicine at the Leiden University Medical Center and subsequently chose the subspecialty of Geriatric Medicine. This is where she started her research into aging.
Exclusive Perks
Convenience
Consistency
Time-Saving