
Den 12. januar 2023 blev der offentliggjort en banebrydende undersøgelse, som ændrer den måde, vi tænker på aldring. Hvis du mener, at aldring er et uundgåeligt evolutionært forløb, og at titlen på denne side er skamløs clickbait, vil sammenfatningen af denne nye publikation måske ændre dit perspektiv.
Denne banebrydende publikation er resultatet af forskellige eksperimenter, der er blevet udført i løbet af det seneste årti. Den repræsenterer en vigtig milepæl, der ændrer den måde, forskere vil designe studier af aldringsforskning på, og kan også hjælpe med at udvikle en ensartet tilgang til behandling af aldersrelaterede sygdomme.
Sammenfatning
Forfatterne til denne artikel brugte en velformuleret, stemningsfuld metafor til at skitsere de vigtigste resultater i denne relativt komplekse publikation:
- Pattedyrenes genom kan betragtes som vores biologiske hardware.
- Epigenomet kan betragtes som vores software. Det påvirker ikke hardwaren, men snarere den måde, vi bruger vores hardware på.
- Indtil nu har vi troet, at nedbrydning af hardware (dvs. DNA-skader) er hovedårsagen til aldring.
- Resultaterne af denne undersøgelses eksperimenter tyder på det modsatte. Softwaren ser ud til at drive den biologiske aldringsproces.
- Forskerne ødelagde laboratoriemusenes software, mens de sørgede for, at deres hardware forblev upåvirket. En accelereret aldringsproces blev observeret. En banebrydende opdagelse!
Men det bliver endnu bedre:
- Derudover brugte de genterapi til at genoprette musenes software til en tidligere, mere ungdommelig tilstand.
- De ved ikke, om det virkede, men det gjorde det, og det tyder på, at musens celler har en sikkerhedskopi af deres software.
- Hvis deres software bliver ødelagt på grund af naturlige aldringsprocesser, kan vi simpelthen genoprette deres ungdommelighed ved hjælp af cellens sikkerhedskopi.
Alt i alt er det en spændende nyhed, da det er meget nemmere at reparere vores software end at reparere eller udskifte hardwaren.
Ordliste
For at få mest muligt ud af vores undersøgelsesoversigt længere nede anbefaler vi, at du sætter dig ind i følgende begreber:
| Betegnelse | Forklaring |
| Epigenetik | refererer til studiet af ændringer i genaktivitet, som ikke involverer ændringer i den underliggende DNA-sekvens. Disse ændringer kan påvirke, hvordan gener udtrykkes eller tændes eller slukkes i forskellige celler, og de kan påvirkes af en persons miljø, livsstil og andre faktorer. De epigenetiske egenskaber er det, der adskiller en celle fra en nervecelle, og aktiveringen eller deaktiveringen af forskellige gener i en celle er også det, der adskiller en blodcelle fra en nervecelle. |
| Trofast DNA-reparation | refererer til den proces, hvor cellerne reparerer fejl eller skader på DNA-molekylet for at bevare den genetiske kodes integritet. Trofast betyder, at reparationsprocessen udføres korrekt og ikke forårsager DNA-mutationer. |
| DNA-mutationer | henviser til ændringer i DNA-sekvensen, som kan forekomme naturligt eller som følge af udsættelse for visse miljøfaktorer som f.eks. stråling eller kemikalier. Nogle mutationer kan forårsage genetiske lidelser eller øge risikoen for visse sygdomme. |
| DNA-methyleringsur | er en biologisk markør, der afspejler ophobningen af epigenetiske ændringer i DNA over tid. Dette ur kan bruges til at estimere alderen på en celle, et væv eller en organisme. Det er en parameter, som kan bruges til at estimere vores biologiske alder. |
| Cellulær identitet | refererer til de egenskaber, der definerer en bestemt celletype, såsom dens form, størrelse, funktion og genekspressionsmønstre. |
| ICE (inducerbar ændringer i epigenomet) | refererer til den proces, hvor miljømæssige eller andre faktorer kan forårsage ændringer i de epigenetiske mærker på en persons DNA, hvilket kan påvirke udtrykket af visse gener og potentielt føre til sygdom. |
Baggrund for undersøgelsen
Denne internationale undersøgelse med titlen Loss of epigenetic information as a cause of mammalian aging var 13 år undervejs og blev endelig offentliggjort den 12. januar i Cell Journal. Den er forfattet af et internationalt team, herunder David Sinclair, professor i genetik fra Harvard Medical School, som er kendt for sin banebrydende forskning i aldring og supplerer NMN med en daglig dosis på 1 gram. Publikationen beskriver adskillige eksperimenter, der er blevet udført for at identificere årsagerne til aldring på et molekylært niveau.
Hvilke kosttilskud tager Dr. Sinclair? Læs hans longevity rutine
Tidligere resultater og RCM-hypotesen
- Forskere har tidligere sat aldring i forbindelse med dobbeltstrengede DNA-brud, som sker i omkring 10 til 50 celler om dagen.
- I den senere tid er der dog blevet sat spørgsmålstegn ved, om DNA-mutationer faktisk er den primære årsag til aldring. Flere fund tyder på, at der kan være mere i historien.
- Forskellige typer af ældre celler viste sig at have meget få mutationer, og nogle mus eller mennesker har ikke vist sig at ældes for tidligt.
- Desuden indikerede resultaterne fra gærstudier fra 1997, at tab af epigenetisk information, snarere end genetisk, potentielt kan forårsage aldring.
- Efterfølgende blev epigenetiske ændringer også sat i forbindelse med aldring hos dyr som fluer, orme og nøgenmuldvarper.
Det fik Dr. Sinclair og hans team til at skabe "RMC (Relocalization of Chromatin Modifiers)-hypotesen.
RCM-hypotesen antager, at aldring i dyreceller er resultatet af tab af epigenetisk information og transkriptionelle netværk over tid. Den underliggende mekanisme, der forårsager dette, udviklede sig til at samregulere vores reaktion på cellulære skader som dobbeltstrengede DNA-brud (DSB'er).
Sådan tester ICE RCM-hypotesen
For at teste denne hypotese udviklede forskerne metoder, der gjorde det muligt for dem først at nedbryde og derefter nulstille den epigenetiske information både in vitro (i celler) og in vivo (i mus).
Det vigtigste eksperiment bestod i at skabe midlertidige brud i laboratoriemusenes DNA. Disse brud var designet til at efterligne de små brud på kromosomerne, som sker i vores og musenes celler hver dag over tid som reaktion på udsættelse for sollys, kemikalier, kosmiske stråler og andre miljøfaktorer.
Husk, at de vil teste, hvordan epigenetiske ændringer påvirker aldring, så disse brud var designet til kun at ændre epigenomet, så de blev ikke udført inden for den kodende region af musenes DNA for at forhindre genmutationer (dvs. ikke-mutagene brud).
Den nyudviklede metode til disse forsætlige kromosombrud blev kaldt ICE-systemet. Testpersonerne fik det passende kælenavn ICE-mus.
Så hvis RCM-hypotesen er korrekt, bør disse mutagene nedskæringer fremskynde den epigenetiske aldring af ICE-musene og også fremskynde andre aldersrelaterede egenskaber sammenlignet med deres nære slægtninge (kontrolgruppen, der ikke blev udsat for nogen nedskæringer).
Hvad skete der, efter at musene havde fået disse pauser?
Til at begynde med var deres adfærd, aktivitetsniveau og fødeindtag ikke anderledes end hos de negative kontrolpersoner. Efter et brud skiftede de epigenetiske faktorer simpelthen fokus fra at regulere gener til at koordinere reparationen af DNA-bruddet. Når bruddet var repareret, vendte de tilbage til deres gamle job med at regulere gener.
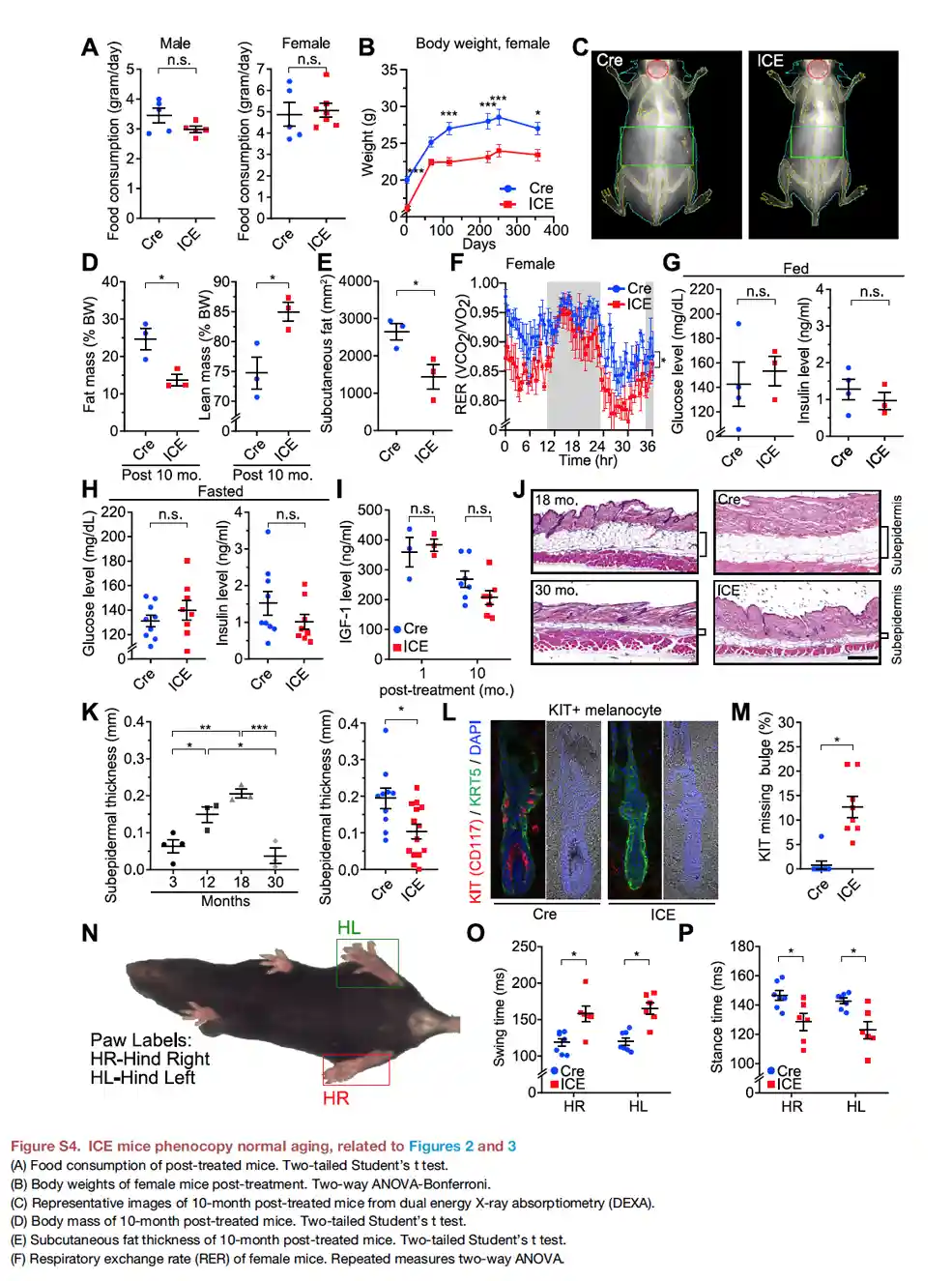
Men efter 1 måned med ICE begyndte der at ske nogle ændringer. ICE-musene udviklede hårtab og mistede pigmenter på næse, ører, fødder og hale. Disse fysiologiske ændringer er typisk forbundet med midaldrende mus.
Efter 10 måneder tabte ICE-musene også kropsvægt, havde et lavere åndedrætsudvekslingsforhold og bevægede sig mindre i den mørke fase. Alt dette er typiske karakteristika, der indikerer alderdom hos mus. Resultaterne under mikroskopet var i overensstemmelse med disse observationer: Forskerne bemærkede, at de førnævnte epigenetiske faktorer ikke vendte tilbage til deres job efter at have repareret DNA-brud. Det resulterede i kaos og funktionsfejl i epigenomet.
Selv om vi allerede kan være ret sikre på, at ICE-musene faktisk blev ældre hurtigere. Forskerne gik et skridt videre og brugte et værktøj udviklet af deres laboratorium, som gjorde det muligt for dem at måle musenes biologiske alder. DNA-methyleringsuret kan bruges på celler, væv eller organismer. ICE-musenes biologiske alder var betydeligt højere sammenlignet med de ubehandlede negative kontroller.
For at opsummere viste eksperimentet, at de ikke-mutagene DNA-brud i mus, som efterligner DNA-brud i hverdagen:
- Fremskynde aldring som indikeret af fysiologiske ændringer, såsom hårtab, tab af pigmentering, lavere kropsvægt, lavere bevægelse i mørke faser og et lavere RER (respiratorisk udvekslingsforhold).
- Hurtigere aldring som defineret af DNA-methyleringsuret, der måler alder biologisk og ikke kronologisk.
- Påvirkede det epigenetiske landskab negativt, når epigenetiske faktorer ikke vendte tilbage til DNA-regulering efter at have reguleret reparationer af inducerede DNA-brud.
Disse resultater understøtter antagelserne i RCM-hypotesen.
Foryngelse af ICE-mus
Men på dette tidspunkt kunne forskerne endnu ikke være sikre på, at DNA-mutationer ikke forårsagede disse effekter. For at udelukke denne mulighed var de nødt til at nulstille epigenomet i både in vivo- og in vitro-eksperimenter.
For at udføre denne "genterapi" for at genoprette epigenomet gav de tre gener kendt som Oct4, Sox2 og Klf4. Trioen kaldes OSK. Disse gener tændes normalt under embryonaludviklingen og er naturligt til stede i stamceller. De hjælper modne celler med at vende tilbage til en mere ungdommelig tilstand.
Sjovt nok var Sinclairs laboratorium i 2020 i stand til at genskabe synet hos blinde laboratoriemus ved hjælp af disse tre gener
Resultaterne af denne genterapi
ICE-musenes væv og organer blev med succes gendannet til en tidligere tilstand, der er forbundet med ungdommelighed. Vi ved endnu ikke, hvordan OSK-baseret genterapi opnår dette, men alt, hvad vi ved, er, at det virker. Vi ved også, at det kræver en sikkerhedskopi at gendanne data. Da sikkerhedskopien ikke kan være inde i OSK-generne, skal den være inde i ICE-musenes pattedyrsceller. Med andre ord: Musenes celler indeholder en potentiel ungdomskilde, og vi har fundet en måde at få adgang til den på!
Hvad man kan tage med sig
Forskerens omfattende sæt af eksperimenter bekræfter, at hovedårsagen til aldring ikke er DNA-forandringer. I stedet synes aldring at være drevet af ændringer i strukturen af kromatin, som er en epigenetisk faktor, der er ansvarlig for dannelsen af kromosomer.
For anti-aging-forskere er disse nye resultater ekstremt opløftende og spændende, fordi manipulation af molekyler, der styrer epigenetiske faktorer, er meget lettere end at vende DNA-mutationer. Undersøgelsen viste, at vi præcist kan kontrollere musenes alder. Vi kan fremskynde den, bremse den eller vende den om, som vi ønsker.
Publikationen viste desuden, at musens pattedyrsceller gemmer en sikkerhedskopi af deres epigenetiske information. Ved hjælp af tre gener kendt som OSK blev epigenomet gendannet til en ungdommelig status ved hjælp af denne sikkerhedskopi.
Ville genterapi med ICE og OSK virke i mennesker?
Laboratoriemus har mange ligheder med mennesker med hensyn til genetik og fysiologi. Men der er også betydelige forskelle mellem de to arter, som man skal tage højde for, når man fortolker resultaterne af prækliniske undersøgelser.
En stor forskel er, at mus har en meget kortere levetid end mennesker, hvilket kan påvirke udviklingen og forløbet af visse sygdomme. Derudover kan størrelsen og organiseringen af visse organer, som f.eks. hjernen, være forskellig mellem de to arter.
På trods af disse forskelle er mange af de cellulære og molekylære processer, der forekommer i mus, også til stede i mennesker, hvilket gør dem til nyttige modeller til undersøgelse af menneskelige sygdomme. Da mennesker og mus er meget ens på celleniveau (begge er pattedyrsceller), er det sandsynligt, at menneskeceller også har sikkerhedskopier af deres epigenom.
På vej fremad
ICE-metoden er en vigtig milepæl for forskningen i anti-aging. Fremtidige eksperimenter med musenes epigenom vil sandsynligvis være mere omkostnings- og tidseffektive, da ICE-musene bliver "gamle" efter kun seks måneder i stedet for de sædvanlige 1,5 til 2 år.
Der bør udføres yderligere eksperimenter for at finde ud af, hvordan OSK-genterapi fremkalder det bemærkelsesværdige "foryngelsesprogram", der er observeret hos mus. Måske kan man finde andre og mere effektive måder at genoprette den epigenetiske backup på.
Forskerne håber, at denne publikation ikke kun vil inspirere forskere til at lære mere om, hvordan vi kan kontrollere vores biologiske alder, men også til at forebygge sygdomme og tilstande, der er forbundet med moden alder, såsom type 2-diabetes, neurodegenerative sygdomme og hjerte-kar-sygdomme (den største dræber i de fleste lande).
Et overbevisende forsøg på mennesker med NMN-tilskud: Fortsæt med at læse denne lovende undersøgelse af NMN.

Spor 50+ sundhedsmålinger med AI-drevet nøjagtighed. Start din gratis prøveperiode i dag, og tag kontrol over din wellness-rejse!

longevity Tips bedste øvelser ernæring kostvaner sund livsstil
Kunsten at leve godt - et liv, der ikke måles i år alene, men i oplevelser, sundhed og glæde!












