
Op 12 januari 2023 werd een baanbrekend onderzoek gepubliceerd dat onze kijk op veroudering verandert. Als u veroudering beschouwt als een onvermijdelijk evolutionair proces en de titel van deze pagina als schaamteloze clickbait, dan kan de samenvatting van deze nieuwe publicatie uw perspectief wellicht veranderen.
Deze baanbrekende publicatie is het resultaat van diverse experimenten die de afgelopen tien jaar zijn uitgevoerd. Het is een belangrijke mijlpaal die de manier verandert waarop wetenschappers onderzoek naar veroudering opzetten, en kan bovendien bijdragen aan de ontwikkeling van een uniforme aanpak voor de behandeling van leeftijdsgebonden ziekten .
Samenvatting
De auteurs van dit artikel gebruikten een goed doordachte, suggestieve metafoor om de belangrijkste bevindingen van deze relatief complexe publicatie te schetsen:
- Het genoom van zoogdieren kan worden beschouwd als onze biologische hardware.
- Het epigenoom kan worden beschouwd als onze software. Het heeft geen invloed op de hardware zelf, maar wel op de manier waarop we onze hardware gebruiken.
- Tot nu toe dachten we dat een defect in de hardware (oftewel DNA-schade) de belangrijkste oorzaak van veroudering is.
- De resultaten van de experimenten in dit onderzoek suggereren het tegenovergestelde. De software lijkt juist het biologische verouderingsproces te stimuleren.
- De onderzoekers verstoorden de software van de laboratoriummuizen, terwijl ze ervoor zorgden dat de hardware intact bleef. Er werd een versneld verouderingsproces waargenomen. Een baanbrekende ontdekking!
Maar het wordt nog beter:
- Daarnaast gebruikten ze gentherapie om de genetische software van de muizen terug te brengen naar een eerdere, jeugdigere staat.
- Ze weten niet of dit werkte, maar het werkte wel, en dit suggereert dat de cellen van muizen een back-upkopie van hun software bewaren.
- Als hun software door natuurlijke verouderingsprocessen beschadigd raakt, kunnen we die eenvoudig herstellen met behulp van de back-up van de telefoon.
Al met al is dit fantastisch nieuws, want het oplossen van softwareproblemen is veel eenvoudiger dan het repareren of vervangen van de hardware.
Woordenlijst
Om het meeste uit onze samenvatting van het onderzoek hieronder te halen, raden we u aan vertrouwd te raken met de volgende termen:
| Termijn | Uitleg |
| Epigenetica | Dit verwijst naar de studie van veranderingen in genactiviteit die geen veranderingen in de onderliggende DNA-sequentie met zich meebrengen. Deze veranderingen kunnen van invloed zijn op hoe genen tot expressie komen, oftewel hoe ze aan- of uitgeschakeld worden, in verschillende cellen en kunnen worden beïnvloed door iemands omgeving, levensstijl en andere factoren. De epigenetische eigenschappen van een cel, en de activering of deactivering van verschillende genen binnen een cel, is ook wat een bloedcel onderscheidt van een zenuwcel. |
| Betrouwbare DNA-reparatie | Dit verwijst naar het proces waarbij cellen fouten of beschadigingen aan het DNA-molecuul herstellen om de integriteit van de genetische code te behouden. 'Fijn' betekent dat het herstelproces correct wordt uitgevoerd en geen DNA-mutaties veroorzaakt. |
| DNA-mutaties | Mutaties verwijzen naar veranderingen in de DNA-sequentie die van nature kunnen optreden of als gevolg van blootstelling aan bepaalde omgevingsfactoren, zoals straling of chemicaliën. Sommige mutaties kunnen genetische aandoeningen veroorzaken of het risico op bepaalde ziekten verhogen. |
| DNA-methyleringsklok | Het is een biologische marker die de accumulatie van epigenetische veranderingen in DNA in de loop van de tijd weerspiegelt. Deze klok kan worden gebruikt om de leeftijd van een cel, weefsel of organisme te schatten. Het is een parameter die kan worden gebruikt om onze biologische leeftijd te bepalen. |
| Cellulaire identiteit | Dit verwijst naar de kenmerken die een bepaald celtype definiëren, zoals de vorm, grootte, functie en genexpressiepatronen. |
| ICE (induceerbaar) veranderingen in het epigenoom) | Dit verwijst naar het proces waarbij omgevingsfactoren of andere factoren veranderingen kunnen veroorzaken in de epigenetische markeringen op het DNA van een persoon, wat de expressie van bepaalde genen kan beïnvloeden en mogelijk tot ziekte kan leiden. |
Achtergrond van de studie
Deze internationale studie , getiteld 'Verlies van epigenetische informatie als oorzaak van veroudering bij zoogdieren', heeft dertien jaar in beslag genomen en werd uiteindelijk op 12 januari gepubliceerd in het tijdschrift Cell. Het onderzoek werd uitgevoerd door een internationaal team, waaronder David Sinclair, hoogleraar genetica aan de Harvard Medical School, die bekendstaat om zijn baanbrekend onderzoek naar veroudering en dagelijks 1 gram NMN-supplementen gebruikt. De publicatie beschrijft talloze experimenten die zijn uitgevoerd om de oorzaken van veroudering op moleculair niveau te achterhalen.
Welke supplementen gebruikt Dr. Sinclair? Lees meer over zijn routine voor een lang leven.
Eerdere bevindingen en de RCM-hypothese
- Onderzoekers hebben veroudering eerder in verband gebracht met breuken in dubbelstrengs DNA, die dagelijks in ongeveer 10 tot 50 cellen voorkomen.
- De laatste tijd zijn er echter vragen gerezen over de vraag of DNA-mutaties wel de voornaamste oorzaak van veroudering zijn. Verschillende onderzoeken suggereren dat er wellicht meer aan de hand is.
- Er is gebleken dat verschillende soorten oudere cellen zeer weinig mutaties bevatten, en bij sommige muizen of mensen is geen sprake van vroegtijdige veroudering.
- Daarnaast wezen de resultaten van giststudies uit 1997 erop dat verlies van epigenetische informatie, in plaats van genetische informatie, mogelijk veroudering kan veroorzaken.
- Vervolgens werden epigenetische veranderingen ook in verband gebracht met veroudering bij dieren zoals vliegen, wormen en naakte molratten.
Dit bracht Dr. Sinclair en zijn team ertoe de "RMC (Relocalization of Chromatin Modifiers)-hypothese" te ontwikkelen.
De RCM-hypothese veronderstelt dat veroudering in dierlijke cellen het gevolg is van het verlies van epigenetische informatie en transcriptionele netwerken in de loop van de tijd. Het onderliggende mechanisme dat dit veroorzaakt, is geëvolueerd om onze reactie op cellulaire schade, zoals dubbelstrengs DNA-breuken (DSB's), te co-reguleren.
Hoe ICE de RCM-hypothese test
Om deze hypothese te testen, ontwikkelden de onderzoekers methoden waarmee ze de epigenetische informatie eerst konden afbreken en vervolgens herstellen, zowel in vitro (in cellen) als in vivo (in muizen).
Het belangrijkste experiment bestond uit het aanbrengen van tijdelijke breuken in het DNA van de laboratoriummuizen. Deze breuken waren bedoeld om de kleine breuken in chromosomen na te bootsen die dagelijks in onze cellen en in de cellen van deze muizen ontstaan als gevolg van blootstelling aan zonlicht, chemicaliën, kosmische straling en andere omgevingsfactoren.
Bedenk dat ze willen testen hoe epigenetische veranderingen veroudering beïnvloeden. Deze breuken waren daarom zo ontworpen dat ze alleen het epigenoom veranderden en werden dus niet aangebracht in het coderende gebied van het DNA van de muizen om genmutaties te voorkomen (oftewel, niet-mutagene breuken).
De nieuw ontwikkelde methode voor deze opzettelijke chromosoombreuken werd het ICE-systeem genoemd. De proefdieren kregen de toepasselijke bijnaam ICE-muizen.
Als de RCM-hypothese correct is, zouden deze mutagene breuken de epigenetische veroudering van de ICE-muizen moeten versnellen, evenals andere leeftijdsgebonden kenmerken, in vergelijking met hun naaste verwanten (de controlegroep die niet aan dergelijke breuken is blootgesteld).
Wat gebeurde er nadat de muizen deze breuken hadden opgelopen?
Aanvankelijk verschilden hun gedrag, activiteitsniveau en voedselconsumptie niet in vergelijking met de negatieve controlegroep. Na een breuk verschoven de epigenetische factoren hun focus van het reguleren van genen naar het coördineren van de reparatie van de DNA-breuken. Nadat de breuk was hersteld, keerden ze terug naar hun oude taak: het reguleren van genen.
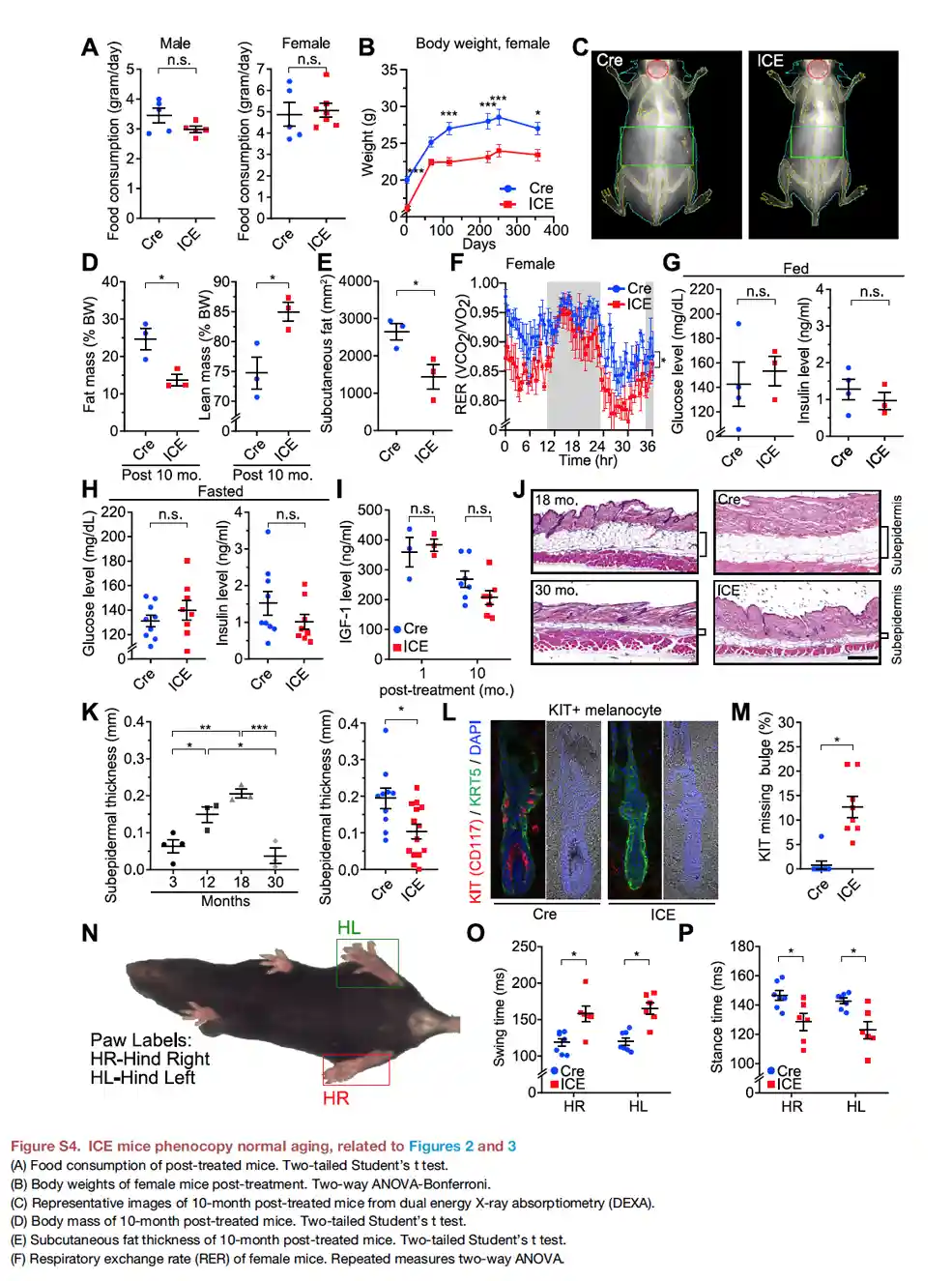
Na een maand ICE begonnen er echter enkele veranderingen op te treden. De ICE-muizen kregen haaruitval en verloren pigment op hun neus, oren, poten en staart. Deze fysiologische veranderingen worden doorgaans geassocieerd met muizen van middelbare leeftijd.
Na 10 maanden verloren de ICE-muizen ook lichaamsgewicht, hadden ze een lagere respiratoire uitwisselingsratio en vertoonden ze minder beweging in de donkere fase. Dit zijn allemaal typische kenmerken die wijzen op ouderdom bij muizen. De bevindingen onder de microscoop waren consistent met deze observaties: de onderzoekers merkten op dat de eerdergenoemde epigenetische factoren niet terugkeerden naar hun oorspronkelijke functie na het herstellen van DNA-breuken. Dit resulteerde in chaos en disfunctie binnen het epigenoom.
Hoewel we er al vrij zeker van kunnen zijn dat de ICE-muizen inderdaad sneller verouderden, gingen de onderzoekers een stap verder en gebruikten ze een door hun laboratorium ontwikkeld instrument waarmee ze de biologische leeftijd van de muizen konden meten. De DNA-methylatieklok kan worden toegepast op cellen, weefsels of organismen. De biologische leeftijd van de ICE-muizen was significant hoger in vergelijking met de onbehandelde negatieve controlegroep.
Samenvattend toonde het experiment aan dat de niet-mutagene DNA-breuken bij muizen, die DNA-breuken in het dagelijks leven nabootsen:
- Versnel het verouderingsproces, zoals blijkt uit fysiologische veranderingen zoals haaruitval, verlies van pigmentatie, een lager lichaamsgewicht, minder beweging tijdens donkere periodes en een lagere RER (respiratoire uitwisselingsverhouding).
- Versnelde veroudering zoals gedefinieerd door de DNA-methylatieklok, die de leeftijd biologisch en niet chronologisch meet.
- Het epigenetische landschap werd negatief beïnvloed toen epigenetische factoren niet terugkeerden naar de DNA-regulatie nadat ze de reparatie van geïnduceerde DNA-breuken hadden gereguleerd.
Deze resultaten ondersteunen de aannames van de RCM-hypothese.
Verjonging van ICE-muizen
Op dit punt konden de onderzoekers echter nog niet met zekerheid vaststellen dat DNA-mutaties deze effecten niet veroorzaakten. Om deze mogelijkheid uit te sluiten, moesten ze het epigenoom resetten in zowel in vivo als in vitro experimenten.
Om deze "gentherapie" uit te voeren en zo het epigenoom te herstellen, dienden ze drie genen toe: Oct4, Sox2 en Klf4. Dit trio wordt OSK genoemd. Deze genen worden normaal gesproken geactiveerd tijdens de embryonale ontwikkeling en zijn van nature aanwezig in stamcellen. Ze helpen volwassen cellen terug te keren naar een meer jeugdige staat.
Leuk weetje: In 2020 slaagde het laboratorium van Sinclair erin het zicht van blinde laboratoriummuizen te herstellen met behulp van deze drie genen.
De resultaten van deze gentherapie
De weefsels en organen van de ICE-muizen werden met succes hersteld naar een eerdere staat die geassocieerd wordt met jeugd. We weten nog niet hoe OSK-gebaseerde gentherapie dit bereikt, maar we weten wel dat het werkt. We weten ook dat een back-up nodig is om de gegevens te herstellen. Omdat de back-up niet in de OSK-genen kan worden opgeslagen, moet deze zich in de zoogdiercellen van de ICE-muizen bevinden. Met andere woorden: de cellen van muizen bevatten een potentiële bron van eeuwige jeugd, en we hebben een manier gevonden om die aan te boren!
De belangrijkste conclusies
De uitgebreide experimenten van de onderzoeker bevestigen dat de belangrijkste oorzaak van veroudering niet DNA-veranderingen zijn. Veroudering lijkt eerder te worden veroorzaakt door veranderingen in de structuur van chromatine, een epigenetische factor die verantwoordelijk is voor de vorming van chromosomen.
Voor onderzoekers op het gebied van anti-veroudering zijn deze nieuwe bevindingen buitengewoon bemoedigend en spannend, omdat het manipuleren van moleculen die epigenetische factoren reguleren veel eenvoudiger is dan het terugdraaien van DNA-mutaties. De studie toonde aan dat we de leeftijd van muizen nauwkeurig kunnen controleren. We kunnen deze versnellen, vertragen of terugdraaien, naar believen.
De publicatie toonde verder aan dat de zoogdiercellen van muizen een back-upkopie van hun epigenetische informatie opslaan. Met behulp van drie genen, bekend als OSK, werd het epigenoom hersteld naar een jeugdige staat met behulp van deze back-upkopie.
Zou gentherapie met ICE en OSK bij mensen werken?
Laboratoriummuizen vertonen veel overeenkomsten met mensen op genetisch en fysiologisch gebied. Er zijn echter ook belangrijke verschillen tussen de twee soorten waarmee rekening moet worden gehouden bij de interpretatie van de resultaten van preklinische studies.
Een belangrijk verschil is dat muizen een veel kortere levensduur hebben dan mensen, wat van invloed kan zijn op de ontwikkeling en het verloop van bepaalde ziekten. Daarnaast kunnen de grootte en de structuur van bepaalde organen, zoals de hersenen, verschillen tussen de twee soorten.
Ondanks deze verschillen zijn veel van de cellulaire en moleculaire processen die bij muizen plaatsvinden ook aanwezig bij mensen, waardoor ze nuttige modellen zijn voor het bestuderen van menselijke ziekten. Omdat mensen en muizen op cellulair niveau erg op elkaar lijken (beide zijn zoogdiercellen), is het waarschijnlijk dat menselijke cellen ook reservekopieën van hun epigenoom hebben.
Vooruitkijken
De ICE-methode is een belangrijke mijlpaal in het onderzoek naar verouderingsresistentie. Toekomstige experimenten met het epigenoom van muizen zullen waarschijnlijk kostenefficiënter en tijdbesparender zijn, omdat ICE-muizen al na zes maanden de "oude leeftijd" bereiken in plaats van de gebruikelijke 1,5 tot 2 jaar.
Verder onderzoek is nodig om te bepalen hoe OSK-gentherapie het opmerkelijke "verjongingsprogramma" induceert dat bij muizen is waargenomen. Wellicht kunnen andere, efficiëntere manieren worden gevonden om de epigenetische reserve te herstellen.
De onderzoekers hopen dat deze publicatie wetenschappers niet alleen zal inspireren om meer te leren over hoe we onze biologische leeftijd kunnen beheersen, maar ook om ziekten en aandoeningen die met de ouderdom samenhangen, zoals diabetes type 2, neurodegeneratieve ziekten en hart- en vaatziekten (de belangrijkste doodsoorzaak in de meeste landen), te voorkomen.
Een overtuigende humane studie naar NMN-suppletie: lees verder over deze veelbelovende studie naar NMN.

Volg meer dan 50 gezondheidsgegevens met AI-gestuurde precisie. Start vandaag nog uw gratis proefperiode en neem de controle over uw welzijn!

Tips voor een lang leven, beste oefeningen, voeding, diëten, gezonde levensstijl
De kunst van het goed leven: een leven dat niet alleen wordt afgemeten aan jaren, maar aan ervaringen, gezondheid en vreugde!












