
Le 12 janvier 2023, une étude révolutionnaire a été publiée, qui modifie notre vision du vieillissement. Si vous pensez que le vieillissement est une évolution inévitable et que le titre de cette page est un clickbait éhonté, le résumé de cette nouvelle publication pourrait changer votre point de vue.
Cette publication pionnière est le résultat de diverses expériences menées au cours de la dernière décennie. Elle représente une étape majeure qui modifie la façon dont les scientifiques concevront les études sur le vieillissement et pourrait également contribuer à l'élaboration d'une approche uniforme du traitement des maladies liées à l'âge.
Résumé
Les auteurs de ce document ont utilisé une métaphore bien conçue et évocatrice pour présenter les principales conclusions de cette publication relativement complexe :
- Le génome des mammifères peut être considéré comme notre matériel biologique.
- L'épigénome peut être considéré comme notre logiciel. Il n'a pas d'incidence sur le matériel, mais plutôt sur la façon dont nous l'utilisons.
- Jusqu'à présent, nous pensions qu'une défaillance du matériel (c'est-à-dire des dommages à l'ADN) était la principale cause du vieillissement.
- Les résultats des expériences menées dans le cadre de cette étude suggèrent le contraire. Le logiciel semble être le moteur du processus de vieillissement biologique.
- Les chercheurs ont corrompu le logiciel des souris de laboratoire tout en s'assurant que leur matériel n'était pas affecté. Un processus de vieillissement accéléré a été observé. Une découverte révolutionnaire !
Mais il y a mieux encore :
- En outre, ils ont utilisé la thérapie génique pour restaurer le logiciel des souris à un état antérieur et plus jeune.
- Ils ne savent pas si cela a fonctionné, mais c'est le cas, et cela suggère que les cellules des souris conservent une copie de sauvegarde de leur logiciel.
- Si leur logiciel est corrompu par les processus naturels de vieillissement, nous pouvons simplement restaurer leur jeunesse en utilisant la copie de sauvegarde de la cellule.
Dans l'ensemble, il s'agit d'une bonne nouvelle, car il est beaucoup plus facile de réparer nos logiciels que de réparer ou de remplacer le matériel.
Glossaire
Pour tirer le meilleur parti de notre résumé d'étude, nous vous recommandons de vous familiariser avec les termes suivants :
| Durée | Explication |
| Épigénétique | désigne l'étude des changements dans l'activité des gènes qui n'impliquent pas de modifications de la séquence d'ADN sous-jacente. Ces changements peuvent affecter la façon dont les gènes sont exprimés, ou activés ou désactivés, dans différentes cellules et peuvent être influencés par l'environnement, le mode de vie et d'autres facteurs. Les propriétés épigénétiques sont ce qui caractérise la cellule, et l'activation ou la désactivation de divers gènes au sein d'une cellule est également ce qui différencie une cellule sanguine d'une cellule nerveuse. |
| Une réparation fidèle de l'ADN | désigne le processus par lequel les cellules réparent les erreurs ou les dommages causés à la molécule d'ADN afin de maintenir l'intégrité du code génétique. Fidèle signifie que le processus de réparation est correctement mené et ne provoque pas de mutations de l'ADN. |
| Mutations de l'ADN | Les mutations sont des changements dans la séquence de l'ADN qui peuvent se produire naturellement ou à la suite d'une exposition à certains facteurs environnementaux tels que les radiations ou les produits chimiques. Certaines mutations peuvent provoquer des troubles génétiques ou augmenter le risque de certaines maladies. |
| Horloge de méthylation de l'ADN | est un marqueur biologique qui reflète l'accumulation des changements épigénétiques au fil du temps dans l'ADN. Cette horloge peut être utilisée pour estimer l'âge d'une cellule, d'un tissu ou d'un organisme. C'est un paramètre qui peut être utilisé pour estimer notre âge biologique. |
| Identité cellulaire | désigne les caractéristiques qui définissent un type particulier de cellule, telles que sa forme, sa taille, sa fonction et ses schémas d'expression génétique. |
| ICE (inducible modifications de l'épigénome) | désigne le processus par lequel des facteurs environnementaux ou autres peuvent entraîner des modifications des marques épigénétiques sur l'ADN d'une personne, ce qui peut affecter l'expression de certains gènes et potentiellement conduire à une maladie. |
Contexte de l'étude
Cette étude internationale, intitulée Loss of epigenetic information as a cause of mammalian aging (La perte d'informations épigénétiques comme cause du vieillissement des mammifères), a été réalisée pendant 13 ans et a finalement été publiée le 12 janvier dans le Cell Journal. Elle a été rédigée par une équipe internationale, dont David Sinclair, professeur de génétique à la Harvard Medical School, réputé pour ses recherches novatrices sur le vieillissement et qui prend du NMN à raison d'un gramme par jour. La publication détaille de nombreuses expériences menées pour identifier les causes du vieillissement au niveau moléculaire.
Quels suppléments le Dr Sinclair prend-il ? Lire son programme de longévité
Résultats antérieurs et hypothèse du MCR
- Les chercheurs ont déjà établi un lien entre le vieillissement et les cassures de l'ADN double brin, qui se produisent dans 10 à 50 cellules par jour.
- Récemment, cependant, on s'est demandé si les mutations de l'ADN étaient réellement le principal moteur du vieillissement. De nombreux résultats suggèrent que l'histoire n'est peut-être pas aussi simple que cela.
- Divers types de cellules plus âgées ont été trouvés avec très peu de mutations, et certaines souris ou personnes n'ont pas été trouvées pour vieillir prématurément.
- En outre, les résultats des études sur les levures de 1997 indiquent que la perte d'informations épigénétiques, plutôt que génétiques, peut potentiellement être à l'origine du vieillissement.
- Par la suite, des changements épigénétiques ont également été corrélés au vieillissement chez des animaux tels que les mouches, les vers et les rats taupes nus.
C'est ce qui a conduit le Dr Sinclair et son équipe à créer l'hypothèse de la "relocalisation des modificateurs de la chromatine" (RMC).
L'hypothèse RCM suppose que le vieillissement des cellules animales est le résultat de la perte d'informations épigénétiques et de réseaux transcriptionnels au fil du temps. Le mécanisme sous-jacent à l'origine de ce phénomène a évolué pour coréguler notre réponse aux dommages cellulaires tels que les cassures double brin de l'ADN (DSB).
Comment la CIE teste-t-elle l'hypothèse de l'ICR ?
Pour tester cette hypothèse, les chercheurs ont développé des méthodes qui leur ont permis de dégrader puis de réinitialiser l'information épigénétique à la fois in vitro (dans des cellules) et in vivo (dans des souris).
L'expérience la plus importante consistait à créer des coupures temporaires dans l'ADN des souris de laboratoire. Ces coupures ont été conçues pour imiter les coupures de faible importance dans les chromosomes qui se produisent quotidiennement dans nos cellules et dans les cellules de ces souris, en réponse à l'exposition au soleil, aux produits chimiques, aux rayons cosmiques et à d'autres facteurs environnementaux.
Rappelez-vous qu'ils veulent tester la façon dont les changements épigénétiques affectent le vieillissement. Ces coupures ont donc été conçues pour modifier uniquement l'épigénome et n'ont donc pas été effectuées dans la région codante de l'ADN des souris afin d'éviter les mutations génétiques (coupures non mutagènes).
La nouvelle méthode mise au point pour ces cassures chromosomiques intentionnelles a été baptisée système ICE. Les sujets testés ont été surnommés à juste titre "souris ICE".
Ainsi, si l'hypothèse de la MRC est correcte, ces coupures mutagènes devraient accélérer le vieillissement épigénétique des souris ICE ainsi que d'autres caractéristiques associées à l'âge par rapport à leurs proches parents (le groupe de contrôle qui n'a été soumis à aucune coupure).
Que s'est-il passé après que les souris ont subi ces ruptures ?
Au début, leur comportement, leur niveau d'activité et leur consommation de nourriture ne différaient pas de ceux des témoins négatifs. Après avoir subi une rupture, les facteurs épigénétiques ont simplement cessé de réguler les gènes pour coordonner les réparations des ruptures de l'ADN. Une fois la rupture réparée, ils ont repris leur ancienne tâche de régulation des gènes.
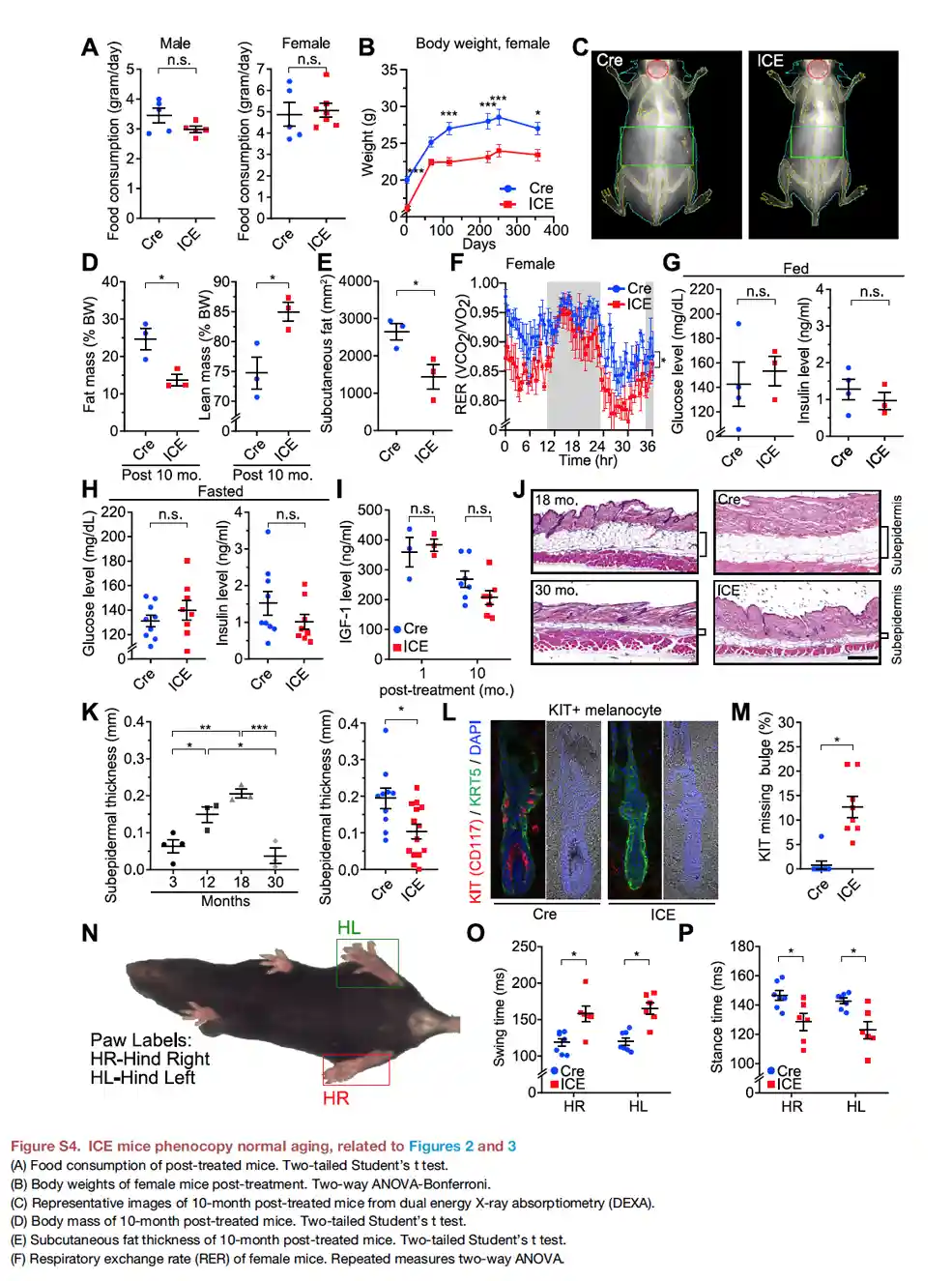
Cependant, après un mois d'ICE, certains changements ont commencé à se produire. Les souris ICE ont commencé à perdre des poils et des pigments sur le nez, les oreilles, les pieds et la queue. Ces changements physiologiques sont généralement associés à des souris d'âge moyen.
Après 10 mois, les souris ICE ont également perdu du poids, leur taux d'échange respiratoire était plus faible et elles bougeaient moins pendant la phase d'obscurité. Toutes ces caractéristiques sont typiques de la vieillesse chez les souris. Les résultats obtenus au microscope concordent avec ces observations : les chercheurs ont remarqué que les facteurs épigénétiques susmentionnés ne reprenaient pas leur fonction après avoir réparé les cassures de l'ADN. Il en résulte un chaos et un dysfonctionnement au sein de l'épigénome.
Si nous pouvons d'ores et déjà être sûrs que les souris ICE ont effectivement vieilli plus vite, les chercheurs sont allés plus loin en utilisant un outil développé par leur laboratoire, qui leur a permis de mesurer l'âge biologique des souris. Les chercheurs sont allés plus loin et ont utilisé un outil développé par leur laboratoire, qui leur a permis de mesurer l'âge biologique des souris. L'horloge de méthylation de l'ADN peut être utilisée sur des cellules, des tissus ou des organismes. L'âge biologique des souris ICE était significativement plus élevé que celui des témoins négatifs non traités.
En résumé, l'expérience a montré que les cassures non mutagènes de l'ADN chez les souris, qui imitent les cassures de l'ADN dans la vie de tous les jours :
- Accélérer le vieillissement, comme l'indiquent les changements physiologiques, tels que la perte de cheveux, la perte de pigmentation, la diminution du poids corporel, la diminution des mouvements pendant les phases sombres et la diminution du RER (ratio d'échange respiratoire).
- Vieillissement accéléré tel que défini par l'horloge de méthylation de l'ADN qui mesure l'âge biologiquement et non chronologiquement.
- Les facteurs épigénétiques ont eu un effet négatif sur le paysage épigénétique lorsqu'ils ne sont pas revenus à la régulation de l'ADN après avoir régulé les réparations des cassures de l'ADN induites.
Ces résultats confirment les hypothèses formulées dans le cadre de l'hypothèse RCM.
Rajeunissement des souris ICE
Toutefois, à ce stade, les chercheurs ne pouvaient pas encore être certains que les mutations de l'ADN n'étaient pas à l'origine de ces effets. Pour écarter cette possibilité, ils ont dû réinitialiser l'épigénome dans des expériences in vivo et in vitro.
Pour mener à bien cette "thérapie génique" visant à restaurer l'épigénome, ils ont administré trois gènes connus sous le nom de Oct4, Sox2 et Klf4. Ce trio est appelé OSK. Ces gènes sont normalement activés au cours du développement embryonnaire et sont naturellement présents dans les cellules souches. Ils aident les cellules matures à retrouver un état plus jeune.
Fait amusant : en 2020, le laboratoire de Sinclair a pu restaurer la vision de souris de laboratoire aveugles en utilisant ces trois gènes.
Les résultats de cette thérapie génique
Les tissus et les organes des souris ICE ont été restaurés avec succès dans un état antérieur associé à la jeunesse. Nous ne savons pas encore comment la thérapie génique basée sur l'OSK y parvient, mais tout ce que nous savons, c'est qu'elle fonctionne. Nous savons également qu'une sauvegarde est nécessaire pour restaurer les données. Comme la sauvegarde ne peut pas se trouver à l'intérieur des gènes OSK, elle doit se trouver à l'intérieur des cellules mammaliennes des souris ICE. En d'autres termes : Les cellules des souris contiennent une fontaine de jouvence potentielle, et nous avons trouvé un moyen d'y accéder !
Les enseignements à tirer
Les nombreuses expériences menées par le chercheur confirment que la principale cause du vieillissement n'est pas l'altération de l'ADN. Au contraire, le vieillissement semble être alimenté par des changements dans la structure de la chromatine, un facteur épigénétique responsable de la formation des chromosomes.
Pour les chercheurs spécialisés dans la lutte contre le vieillissement, ces nouvelles découvertes sont extrêmement encourageantes et passionnantes, car la manipulation des molécules qui contrôlent les facteurs épigénétiques est beaucoup plus facile que l'inversion des mutations de l'ADN. L'étude a montré que nous pouvions contrôler précisément l'âge des souris. Nous pouvons l'accélérer, le ralentir ou l'inverser à notre guise.
La publication a également montré que les cellules mammaliennes des souris conservent une copie de sauvegarde de leurs informations épigénétiques. En utilisant trois gènes connus sous le nom d'OSK, l'épigénome a été restauré à un état de jeunesse en utilisant cette copie de sauvegarde.
La thérapie génique ICE et OSK serait-elle efficace chez l'homme ?
Les souris de laboratoire présentent de nombreuses similitudes avec les humains en termes de génétique et de physiologie. Cependant, il existe également des différences significatives entre les deux espèces qui doivent être prises en compte lors de l'interprétation des résultats des études précliniques.
Une différence majeure est que les souris ont une durée de vie beaucoup plus courte que les humains, ce qui peut affecter le développement et la progression de certaines maladies. En outre, la taille et l'organisation de certains organes, comme le cerveau, peuvent être différentes entre les deux espèces.
Malgré ces différences, de nombreux processus cellulaires et moléculaires qui se produisent chez les souris sont également présents chez les humains, ce qui en fait des modèles utiles pour l'étude des maladies humaines. Étant donné que les humains et les souris sont très similaires au niveau cellulaire (les deux sont des cellules de mammifères), il est probable que les cellules humaines possèdent également des copies de sauvegarde de leur épigénome.
Aller de l'avant
La méthode ICE constitue une étape importante pour la recherche contre le vieillissement. Les expériences futures sur l'épigénome des souris seront probablement plus rentables et plus rapides, puisque les souris ICE entrent dans la "vieillesse" après seulement six mois au lieu des 1,5 à 2 ans habituels.
D'autres expériences devraient être menées pour déterminer comment la thérapie génique OSK induit le remarquable "programme de rajeunissement" observé chez les souris. D'autres moyens plus efficaces de restaurer la sauvegarde épigénétique pourront peut-être être identifiés.
Les chercheurs espèrent que cette publication incitera non seulement les scientifiques à poursuivre leurs recherches sur la manière de contrôler notre âge biologique, mais aussi à prévenir les maladies et les affections associées à l'âge mûr, telles que le diabète de type 2, les maladies neurodégénératives et les maladies cardiovasculaires (la première cause de mortalité dans la plupart des pays).
Une étude humaine convaincante sur la supplémentation en NMN : continuez à lire cette étude prometteuse sur le NMN.

Effectue le suivi de plus de 50 mesures de santé avec une précision alimentée par l'IA. Commence ton essai gratuit dès aujourd'hui et prends le contrôle de ton parcours de bien-être !

conseils de longévité meilleurs exercices régimes alimentaires mode de vie sain
L'art de bien vivre une vie qui ne se mesure pas seulement en années, mais en expériences, en santé et en joie !












